Valsartan
| Artikel ko maagiah informasi dasa tantang topik kasihatan. Informasi dalam artikel ko buliah digunoan anyo untuak panjalehan ilmiah, bukan untuak diagnosis diri dan indak dapek manggantian diagnosis medis. Paratian: Informasi dalam artikel ko bukanlah resep atau nasihaik medis. Wikipedia bukan pangganti dotor. Kok Sanak paralu bantuan atau ka barubek bakonsultasilah jo tanago kasihatan profesional. |
 | |
 | |
| Data klinis | |
|---|---|
| Namo dagang | Diovan, Co Diovan, Valesco, dan lainnyo |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a697015 |
| Lisensi data | |
| Kategori pado kahamilan | |
| Rute masuak ubek | Muluik |
| Kelas ubek | Antagonis reseptor angiotensin II |
| Kode ATC | |
| Status legal | |
| Status legal |
|
| Farmakokinetik data | |
| Bioavailabilitas | 25% |
| Ikatan protein | 95% |
| Eliminasi wakatu paruah | 6 hours |
| Ekskresi | Ginjal 30%, ampadu 70% |
| Pangenal | |
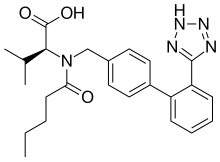
(S)-3-methyl-2-(N-{[2'-(2H-1,2,3,4-tetrazol-5-yl)biphenyl-4-yl]methyl}pentanamido)butanoic acid
| |
| Nomor CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.113.097 |
| Data kimia jo fisika | |
| Formula | C24H29N5O3 |
| Molar mass | 435.519 g/mol g·mol−1 |
| 3D model (JSmol) | |
O=C(O)[C@@H](N(C(=O)CCCC)Cc3ccc(c1ccccc1c2n[nH]nn2)cc3)C(C)C | |
InChI=1S/C24H29N5O3/c1-4-5-10-21(30)29(22(16(2)3)24(31)32)15-17-11-13-18(14-12-17)19-8-6-7-9-20(19)23-25-27-28-26-23/h6-9,11-14,16,22H,4-5,10,15H2,1-3H3,(H,31,32)(H,25,26,27,28)/t22-/m0/s1 Key:ACWBQPMHZXGDFX-QFIPXVFZSA-N | |
| (verify) | |
Valsartan adolah ubek dari golongan antagonis reseptor angiotensin II. Ubek ko bakarajo maambek reseptor angiotensin II sainggo takanan darah manurun dan baguno dek pandarito takanan darah tinggi (hipertensi), gagal jantuang (heart failure), jo panyakik ginjal diabetik (nefropati diabetik).[1] Valsartan tamasuak ubek kareh nan pamakaiannyo musti manyaratokan resep dokter.[2] Valsartan tamasuak pulo dalam ubek kategori D nan aratinyo tabukti barisiko untuak janin.[3]
Valsartan marupokan ubek nan dipakai jo caro diminum (oral) nan babantuak tablet.[1] Di Indonesia ubek ko tasadio dalam bantuak generik dan ado juo dalam bantuak paten jo namo dagang tanamo yaitu Diovan.[3][4] Valsartan tasadio pulo dalam bantuak kombinasi jo hidroklorotiazid, amlodipin, atau sakubitril.[1]
Valsartan dikontraindikasikan pamakaiannyo pado urang nan hipersensitif jo kanduangan ubek ko sarato pandarito diabetes mellitus nan mamakai ubek aliskerin. Valsartan juo indak disarankan pamakaiannyo pado urang jo gangguan ati (hepar) jo gangguan ginjal manangah inggo barek. Efek sampiang nan dapek muncua antaronyo latiah, paniang, kadar potasium tinggi dalam dalam (hiperkalemia), diare, jo sakik di sandi tulang. Efek paliang barek bisa sampai gangguan ginjal, takanan darah randah, jo sambok-sambok badan (angioedema).[1]
Valsartan alah tamasuak dalam Formularium Nasional (Fornas) nan dikaluakan Kementerian Kesehatan Indonesia. Ubek ko juo alah ditangguang dek BPJS Kesehatan jo syaraik pandarito indak dapek mamakai ubek antihipertensi golongan paambek ACE (ACE Inhibitor).[5] Pado taun 2018, babarapo merek dagang valsartan dilarang paredarannyo dek BPOM RI karano bahan bakunyo ado nan tabukti tacemar Nitrosodimethylamine (NDMA) nan bapotensi mamicu kanker (karsionogenik) pado pamakaian jangko lamo.[6]
Sediaan ubek
[suntiang | suntiang sumber]Valsartan marupokan ubek nan dipakai jo caro diminum. Ado duo bantuak sediaan nan ado, yaitu tablet jo oral solution. Banntuak tablet marupokan bantuak nan acok dipakai di Indonesia. Tablet valsartan tasadio dalam dosis 40mg, 80 mg, 160 mg, inggo 320mg. Samantaro bantuak oral solution tasadio dalam dosis 4mg/mL. Bantuak oral solution ko marupokan bantuak cairan.[7]
Indikasi
[suntiang | suntiang sumber]

Valsartan marupokan ubek nan dipakai untuak maubek takanan darah tinggi (hipertensi), gagal jantuang (heart failure), jo panyakik ginjal diabetik. Ubek ko dapek pulo manurunkan risiko kamatian pado urang jo gangguan fungsi ventikel kiri (left ventricular dysfunction) sasudah takanai sarangan jantuang (heart attack).[8][9]
Pado panyakik hipetensi, ubek ko bisa manjadi ubek piliahan partamo saroman ubek antihipertensi lainnyo.[1] Namun, Di Indonesia pado urang nan hipertensi jo Jaminan Kesehatan Nasional (JKN) BPJS hanyo buliah dapek katiko ubek antihipertensinyo indak sasuai lai di dirinyo.[5]
Kontraindikasi
[suntiang | suntiang sumber]Valsartan dikontraindikasikan pado urang diabetes melitus nan mamakai ubek aliskerin.[9]Salain itu, ubek ko dikontraiindikasikan pulo pado urang jo gangguan ginjal. Pado urang manganduang anak baitu pulo. Food and Drugs Administration (FDA) mamasuakan ubek ko dalam kategori D dek efeknyo nan babahayo pado janin nan dikanduang.[9][10] Ubek ko disarankan pulo untuak indak diagiah pado urang nan tangah manyusui.[11]
Farmakologi
[suntiang | suntiang sumber]Valsartan bakarajo jo manyakek karajo angiotensin II nan dapek mampasampik ukuran pambuluah darah sarato maaktivasi aldosteron, sainggo takanan darah dapek turun. Ubek ko ka takabek jo reseptor angiotensin II tipe I nan bakarajo balawanan dari angiotensin II. Salayang, karajo valsartan sarupo jo ubek golongan panyakek ACE (angiotensin-converting enzyme). Namun, nyatonyo babeda. Panyakek ACE bakarajo jo manyakek parubahan angiotensin I manjadi II sainggo dapek maalangi karajo lain dalam tubuah. Samantaro valsartan lansuang pado tampek lakek angiotensin II sainggo efeknyo hanyo pado nan dikandaki sarupo manurunan takanan darah, tapi karajo lain sarupo metabolisme bradikinin indak taganggu.
Valsartan masuak dalam tubuah malalui pamakaian sacaro oral (muluik). Katiko alah masuak dalam tubah, valsartan diedarkan dek protein darah. Ikatan jo protein sangaiklah arek inggo 95%. Efek alsartan dapek muncua dalam duo jam dan batahan inggo 24 jam. Valsartan ka dimetabolisme di hati nan kudian dibuang malalui kotoran (83%) jo urin (13%), jo wakatu paruah 6 jam dalam tubuah.[12][7]
Paredaran
[suntiang | suntiang sumber]Valsartan nan baredar di pasaran tasadio dalam bantuak generik ataupun bantuak paten, baiak hanyo barisi valsartan surang ataupun kombinasi. Valsartan nan baredar dalam bantuak kombinasi ado nan dikombinasikan jo amlodipin atau hidroklorotiazid nan baguno untuak maubek hipertensi jo terapi nan kombinasi.[13][14] Kombinasi lain nan ado yaitu valsartan/sakubitril (valsartan/sacubitril) nan baguno untuak pandarito gagal jantuang jo fraksi ejeksi bakurang (heart failure with reduced ejection fraction).[15][16]
Panarikan
[suntiang | suntiang sumber]Pado 6 Juli 2018, Eupopean Medicines Agency (EMA) malakukan palarangan edar untuak valsartan tongga atau valsartan kombinasi nan baredar di Eropa inggo Kanada.[17] Palarangan edar ko hanyo balaku untuak valsartan nan manggunokan bahan baku buatan Zhejiang Huahai Pharmaceutical Co. (ZHP) di Linhai, Cino. Hal iko dilakukan dengan pado zat aktif tasabuik takontaminasi jo N-nitrosodimetilamin (NDMA) nan karsinogenik (bapotensi mamicu kanker).[18] Diikuti pulo jo FDA (Food and Drug Adminitration; badan ubek Amerika Serikat) untuak malarang paredarannyo.[19] Di Indonesia, BPOM malakukan hal nan samo pulo [6] nan diikuti nagara-nagara lainnyo.[20]
Rujuakan
[suntiang | suntiang sumber]- ↑ a b c d e "Valsartan Monograph for Professionals". Drugs.com. American Society of Health-System Pharmacists. Diakses tanggal 3 March 2019.
- ↑ "Valsartan". Alodokter. 2015-01-15. Diakses tanggal 2020-01-08.
- ↑ a b "VALSARTAN | PIO Nas". pionas.pom.go.id. Diarsipkan dari versi asli tanggal 2020-01-07. Diakses tanggal 2020-01-08.
- ↑ British national formulary : BNF 76 (edisi ke-76). Pharmaceutical Press. 4 Nopember 2018. pp. 179. ISBN 9780857113382.
- ↑ a b "BPJS Kesehatan". bpjs-kesehatan.go.id. Diarsipkan dari versi asli tanggal 2020-01-27. Diakses tanggal 2020-01-08.
- ↑ a b Setyanti, Christina Andhika. "Mengenal Valsartan, Bahan Obat Hipertensi yang Ditarik BPOM". gaya hidup (dalam bahasa Inggris). Diakses tanggal 2020-01-08.
- ↑ a b "Diovan, Prexxartan (valsartan) dosing, indications, interactions, adverse effects, and more". reference.medscape.com. Diakses tanggal 2020-01-28.
- ↑ Randa, Hilal-Dandan (2011). "Chapter 26. Renin and Angiotensin". di dalam Brunton, L. L.; Chabner, Bruce; Knollmann, Björn C.. Goodman & Gilman's The Pharmacological Basis of Therapeutics (edisi ke-12th). New York: McGraw-Hill. ISBN 978-0-07-162442-8.
- ↑ a b c "Diovan prescribing information" (PDF). Novartis.
- ↑ "Valsartan Pregnancy and Breastfeeding Warnings". Drugs.com. Diakses tanggal 3 March 2019.
- ↑ "DIOVAN Product Monograph". Health Canada Drug Product Database. Novartis Pharmaceuticals Canada Inc. Diarsipkan dari versi asli tanggal 23 September 2016. Diakses tanggal 5 November 2015.
- ↑ "Valsartan - Valsartan Tablet". DailyMed. 2017-12-07. Diakses tanggal 2019-02-06.
- ↑ "Search Results for valsartan". DailyMed. Diakses tanggal 2019-02-03.
- ↑ "Amlodipine, Valsartan And Hydrochlorothiazide- Amlodipine, Valsartan And Hydrochlorothiazide Tablet". DailyMed. 2018-02-13. Diakses tanggal 2019-02-03.
- ↑ Fala L (September 2015). "Entresto (Sacubitril/Valsartan): First-in-Class Angiotensin Receptor Neprilysin Inhibitor FDA Approved for Patients with Heart Failure". Ah & Db. 8 (6): 330–334. PMC 4636283
 . PMID 26557227.
. PMID 26557227.
- ↑ Khalil P, Kabbach G, Said S, Mukherjee D (2018). "Entresto, a New Panacea for Heart Failure?". Cardiovascular & Hematological Agents in Medicinal Chemistry. 16 (1): 5–11. doi:10.2174/1871525716666180313121954. PMID 29532764.
- ↑ Christensen J. "Common heart drug recalled in 22 countries for possible cancer link". CNN. Diakses tanggal 14 July 2018.
- ↑ Edney A, Berfield S, Yu E (12 September 2019). "Carcinogens Have Infiltrated the Generic Drug Supply in the U.S." Bloomberg News. Diakses tanggal 17 September 2019.
- ↑ (13 September 2018). FDA provides update on its ongoing investigation into valsartan products; and reports on the finding of an additional impurity identified in one firm's already recalled products. Siaran pers.
- ↑ Harney A, Hirschler B (22 August 2018). "Toxin at heart of drug recall shows holes in medical safety net". Reuters. Diakses tanggal 23 November 2018.
